腾盛博药(02137.HK)近日公布,其新冠中和抗体组合疗法BRII-196/BRII-198在美国国立卫生研究院(NIH)支持的全球大规模III临床研究ACTIV-2中结果积极。对于这家抗感染创新药公司来说,2021年夏天喜事连连,先是在7月成功登陆港交所,又将成为全球又一家上市新冠中和抗体药物的公司。
新冠中和抗体药物市场表现
目前多个国家的新冠疫苗已被授权紧急使用(EUA)或正式批准上市,然而一方面全球范围内疫苗供需极度不均衡,另一方面新冠病毒的快速变异对疫苗带来挑战,两方面导致世界范围内疫情多次反复,至今仍未平息。在此情况下,对新冠肺炎现有及新发病例的治疗十分重要,对因治疗的药物除了“人民的希望”瑞德西韦,另外重要的一类就是新冠中和抗体。
图表1. 全球新冠肺炎每周确诊及死亡病例(2021.8.26更新)
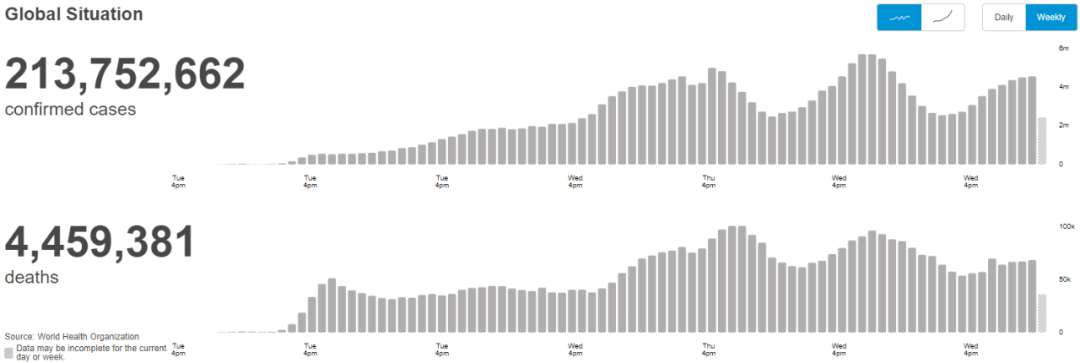
来源:世界卫生组织(WHO),中康产业资本研究中心
与新冠疫苗类似,全球也掀起了针对新冠中和抗体的研发竞赛,迅速将多款产品推上市场。
再生元和罗氏联合开发的新冠中和抗体鸡尾酒疗法REGN-COV(casirivimab/imdevimab)因治愈美国前总统特朗普而名声大噪,在2020年11月被FDA授权紧急使用,2021年上半年全球实现销售额约35.1亿美元。礼来的新冠中和抗体巴尼韦单抗(bamlanivimab,LY-CoV555)单药疗法,以及与君实生物联合开发的埃特司韦单抗(etesevimab,JS016/LY-CoV016)组成的联合疗法分别于2020年11月和2021年2月获得FDA紧急使用授权,2021年上半年的销售额合计约9.6亿美元。Vir Biotechnology和GSK联合开发的新冠中和抗体sotrovimab(VIR-7831)于2021年5月获得FDA紧急使用授权,2021年上半年实现销售额1600万英镑。
总体来看,目前已上市的新冠中和抗体药物应该都能成为2021年的“重磅炸弹”药物,然而彼此间因上市时间、获批国家的差异而在销售额上拉开差距。与新冠疫苗相比,新冠中和抗体药物的销售规模要小得多,但是在新冠疫情持续的情况下不失为能够带来较多收益的好产品。此外,新冠中和抗体不仅具有治疗作用,而且能够短期预防感染,双管齐下的模式对于控制疫情具有非常积极的意义。
新冠中和抗体药物临床数据
腾盛博药的BRII-196/BRII-198是中国目前唯一在全球开展大规模III期临床研究的新冠中和抗体疗法。ACTIV-2试验主方案采用随机、双盲、对照的适应性平台型临床试验设计,预计在全球招募8797例受试者,以评估多种新冠治疗药物的安全性和有效性,其中新冠中和抗体有BRII-196/BRII-198、阿斯利康的AZD7442、BMS的BMS-986414/BMS-986413、SAB Biotherapeutics的SAB-185,以及再生元和罗氏的casirivimab/imdevimab
BRII-196/BRII-198试验组在美国、巴西、南非、墨西哥及阿根廷的研究中心入组837例疾病进展高风险的门诊患者(≥60岁或任何年龄伴有其他疾病),评估能否在研究的28天中达到预防住院或死亡的复合终点。对于69%入组患者的期中分析显示,与安慰剂相比,BRII-196/BRII-198联合疗法使住院及死亡的复合终点降低78%。
图表2. 新冠中和抗体在门诊患者中的临床数据
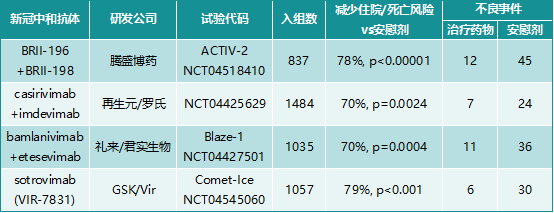
来源:公开资料,中康产业资本研究中心
BRII-196/BRII-198联合疗法在有效性方面,即减少住院或死亡风险,与其他已获批的新冠中和抗体药物相近;在安全性方面略优,既无药物相关严重不良事件或死亡,也没有严重的输注反应。总的来说,临床数据显示腾盛博药的联合疗法与其他新冠中和抗体药物基本相近。腾盛博药目前公布的仅是期中分析数据,如后续数据保持现有趋势甚至更优,那么BRII-196/BRII-198极有可能基于此项III期试验数据获得FDA紧急使用授权。
在国内,腾盛博药于2020年初就与清华大学和深圳市第三人民医院达成合作,共同开发BRII-196和BRII-198。目前,由钟南山院士牵头的II期临床试验(NCT04787211)正在中国进行。在中国的I期和II期试验数据显示联合疗法具有良好的安全性及耐受性。
阿斯利康6月公布了III期暴露后预防临床试验Storm Chaser的结果,未能达到主要终点。8月公布的III期暴露前预防临床试验PROVENT积极结果,相比对照组,AZD7442使有症状新冠肺炎的发病率降低77%。AZD7442是两种长效抗体(AZD8895/AZD1061)的组合,利用专有半衰期延长技术优化,单次肌注可提供12个月的预防性免疫保护。与腾盛博药的联合疗法类似,AZD7442经优化减少Fc受体和补体C1q的结合,将抗体依赖性增强(ADE)风险降至最低。预防成为AZD7442的主攻方向,而非治疗,但是预防作用又面临疫苗的有力竞争。
新冠中和抗体药物的未来竞争
新冠病毒从2019底被发现至今,发生了频繁的变异,包括2020年5月南非首次纪录的贝塔、9月英国首次纪录的阿尔法、10月印度首次纪录的德尔塔、11月巴西首次纪录的伽马等,其中德尔塔突变株株传染性强、重症率高。对于病毒突变株的疗效已经成为新冠中和抗体药物市场的重要影响因素,礼来已经在此方面历经风波。
今年6月,体外数据显示礼来/君实的中和抗体联合疗法对贝塔突变株(B.1.351,南非突变株)和伽马突变株(P.1,巴西突变株)无活性。美国疾控中心(CDC)监测这两种突变株在美国的比例已超过11%,因此美国备灾和应对助理部长(ASPR)办公室和FDA暂停分发礼来的两种中和抗体。然而,随疫情变化,目前美国绝大部分新冠病例已是德尔塔突变株(B.1.617.2/AY.3,印度突变株),而礼来/君实的联合疗法对此突变株有效,因此在8月27日被美国重启分发。
目前的体外嵌合病毒实验数据表明,腾盛博药的BRII-196/BRII-198联合疗法对新冠病毒突变株具有广谱中和活性,包括阿尔法、贝塔、伽马、伊普西龙、德尔塔及拉姆达突变株。此外,GSK/Vir的sotrovimab(VIR-7831)也具有广谱中和活性,凭借GSK的强大市场能力,将会成为有力的竞争对手。
结 语
积极的III期试验数据对于腾盛博药无疑是利好,公告发布当日公司股价应声上涨。对于尚无上市产品,代码仍然冠以字母B的港股新晋生物科技公司,新冠中和抗体联合疗法如能在年内顺利获批,将给公司市值带来新的高峰。然而,新冠中和抗体药物市场受到病毒突变株谱系持续变化,以及新冠疫苗接种情况的影响,具有一定的不确定性。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..