2021年6月22日,ADC Therapeutics宣布,其靶向CD25的新型抗体偶联药物(ADC)camidanlumab tesirine(Cami),在治疗复发/难治性霍奇金淋巴瘤患者的关键性2期临床试验中获得积极结果。中期分析显示,经过大量前期治疗的患者接受Cami治疗后,达到66.3%的总缓解率(ORR)与27.7%的完全缓解率(CRR),且没有出现新的安全性信号。本次研究旨在支持向美国FDA提交生物制品许可申请(BLA)。本次结果显示了Cami解决接受过多种前期治疗的患者未满足需求的潜力。
ADC是一类由靶向特定肿瘤相关抗原的单克隆抗体和偶联在该抗体上的有效载荷构成的新型药物,将单克隆抗体的靶向递送与有效载荷的肿瘤杀伤潜力结合。Camidanlumab tesirine(又名ADCT-301)由能与CD25结合的单克隆抗体,与吡咯苯二氮卓(PBD)二聚体偶联生成。一旦与表达CD25的细胞结合,它就会被细胞内化。在那里,蛋白酶释放基于PBD的有效载荷,杀死细胞。这个过程还可能杀伤邻近的肿瘤细胞,也已被证明可诱导免疫原性细胞死亡。Cami的所有这些特性都可能增强免疫介导的抗肿瘤活性。
正在进行的多中心、开放标签、单组的2期临床试验共入组117例复发/难治性霍奇金淋巴瘤患者,这些患者大部分既往接受过≥3种治疗,包括brentuximab vedotin和免疫检查点抑制剂治疗。本次中期数据基于101例可评估患者,他们接受的前期全身性治疗的中位数为6种,参加研究的中位时间为5.1个月。
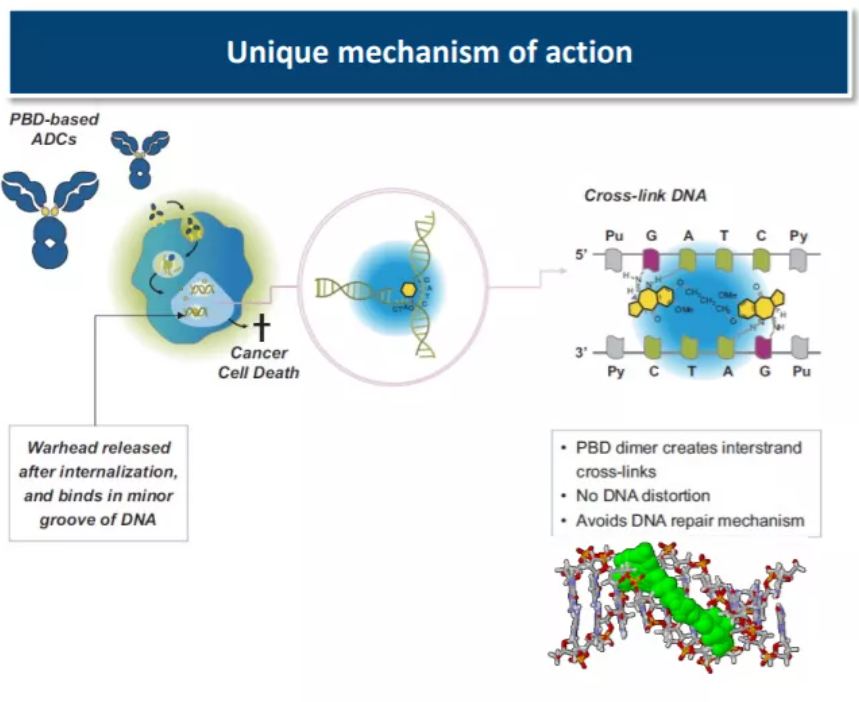
▲吡咯苯二氮卓(PBD)二聚体细胞毒素具有独特的作用机制(图片来源:ADC Therapeutics官网)
中期分析的主要结果包括:
注:原文有删减
参考资料:
[1] ADC Therapeutics Announces Encouraging Interim Results from Pivotal Phase 2 Clinical Trial of Camidanlumab Tesirine (Cami) Presented at the 16th Annual International Conference on Malignant Lymphoma. Retrieved June 22, 2021, from https://www.businesswire.com/news/home/20210622005355/en
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..