一边在创新上攻关,一边用商业来起舞,天境生物的“良性循环”仍在继续。
3月底,天境生物公布了2020年的业绩,全年收入人民币15.43亿元,同比上涨了惊人的5042.23%。对于暂无产品上市的天境生物,财务上的亮眼表现 得益于此前那笔近30亿美元的对外授 权(License-out)交易。
2020年9月,天境生物宣布与跨国巨头艾伯维建立肿瘤免疫创新药的全球战略合作。艾伯维获得了天境自主研发的高度差异化创新CD47单克隆抗体 Lemzoparlimab(TJC4)在大中华区以外的国家及地区开发和商业化许可权。
29.4亿美元的总交易金额刷新了中国生物医药企业海外授权金额的最高纪录,天境生物一鸣惊人。
不只是外界的刮目,靠着两亿美元的首付款和后续里程碑付款,2020年天境生物净利润4.71亿元,相较于2019年亏损14.52亿元,同比增长131.71%,让这家成立不到5年的生物公司首次实现了盈利。
“合作产生的收入不是一次性的,未来将会连续累加下去为天境带来持续的现金流。”天境生物创始人兼董事长臧敬五对《医药界》·E药经理人说道。
“开了一个好头”之后,天境生物的势头又将如何延续,外界半是期待半是好奇。

天境生物创始人兼董事长臧敬五
01 天境2.0:创新结合商业
对于外界的好奇,臧敬五显然是自信的。
“实现从0到1我们用了三年半的时间,而从1到2的转变已经开始了。未来三年内天境生物将从一家处在临床研发阶段的公司转变成为全产业链的、全球的、创新的生物医药公司。”
为了实现这种跨越,天境生物动作不断。
作为去年国内生物医药企业赴美上市的“第一股”,自2020年1月至今,天境生物已经达成了19个研发关键里程碑。
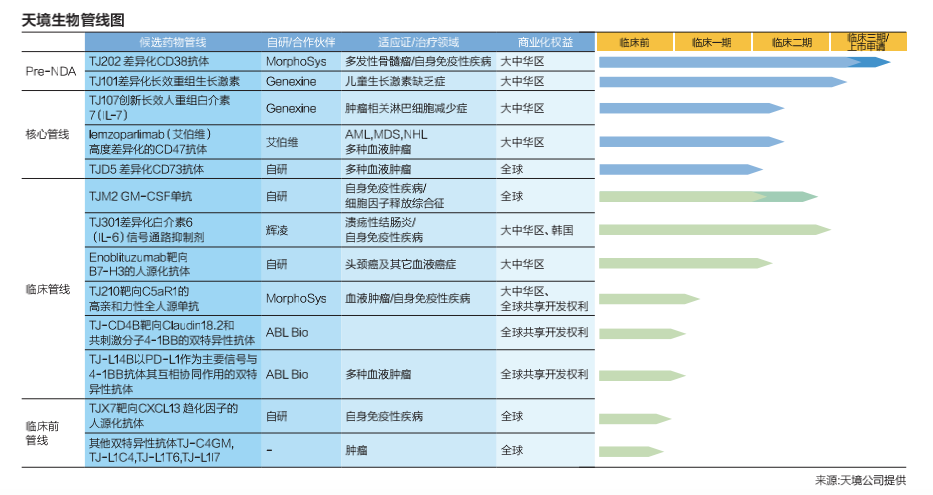
在研发上,目前天境生物拥有16款创新药组成的研发管线,“不仅创新,而且是非常成熟的管线”。臧敬五表示已有两款产品正在进行3项注册临床试验(Pre-NDA),到2021年年底,16款产品中差不多有三分之二会启动Ⅱ/Ⅲ期临床研究。
其中CD38抗体菲泽妥单抗(TJ202)有望从现有研发管线中脱颖而出率先达到注册临床试验终点。
2017年11月,天境 生物与德国MorphoSys签订授权许可协议,拥有了后者的CD38抗体TJ202在中国大陆及港澳台地区的独家开发和商业化权利。天境生物计划在2021年第四季度提交新药上市申请,适用于三线或二线复发性或难治性多发性骨髓瘤(MM)的治疗。
多发性骨髓瘤是一种血液肿瘤,常见于 65~74 岁的老年人群。哈尔滨血液 病肿瘤研究所所长、中国临床肿瘤学会监事会监事长马军教授表示,近年来我国多发性骨髓瘤的发病率增速很快,到2030年,每年可能将会有十万例的新增患者。
多发性骨髓瘤的治疗药物不断更新迭代,目前全球该适应证已上市药物已有十多款,其中百时美施贵宝的超级重磅炸弹来那度胺2020年销售额达到了121.06亿美元。作为全球首款CD38单抗,强生的达雷妥尤单抗同样在多发性骨髓瘤上同样表现不俗,2020年上市第五年的销售已达到41.9亿美元。
2019年达雷妥尤单抗在中国获批。天境生物CEO申华琼介绍,与达雷妥尤单抗相比,菲泽妥单抗输液反应发生率低(7%)、输液时间短(0.5~2小 时),在安全性和注射反应上具有差异化优势。马军表示,“CD38与其他药物联用,MM患者可以实现像糖尿病、高血压一样管理,达到10年的长期生存。 我国每年使用这种疗法的患者数量将有30万。”
“天境生物不仅仅局限在药物创新上,而是要将创新和商业化结合好。”臧敬五说道。
菲 泽 妥 单 抗 、C D 4 7 单 抗lemzoparlimab,加上另一款将授权引进(License-in)处于临床后期的淋巴瘤治疗药物组成了天境生物商业化的第一步。天境生物首席商务官朱益飞表示通过第一波上市的核心产品组合,天境生物将可以覆盖75%的血液肿瘤市场,建立公司在该领域的领导地位。
在不同的阶段实现不同的价值点是天境生物将创新与商业化结合在一起的另一种策略。艾伯维之外,天境生物还和ABL Bio公司、石药集团、乐普医药等公司达成了多项“License-out” 交易。“这些转让为公司提供了现金流,最晚到2023年会跟产品的销售收入叠加,为创新提供持续的支持。”臧敬五指出。
除此之外,据了解天境生物正在杭州建一个全球标准的GMP生产基地,赋能未来在中美两国的临床开发和上市产品的生产。预计2022年前完成两条中式生产线(2x2000L和1x2000L),到2023年年底前将配备4000L的产能,后续商业化生产规模将根据产品上市需求逐渐扩大。
天境生物同时还在组建商业化团队,包括市场准入、医学策略、市场策略等各个方面。朱益飞对《医药界》·E药经理人表示,“团队的核心成员基本已经招募到位,后续整体商业化的进程将会大大提升。”
据透露,天境生物计划在香港或科创板进行第二次上市,“连接中国整个资本市场助推药物创新。”
02 创新第三波:差异化与超级抗体
说到底,还是要回到创新。
不过,什么是真正的创新、First-in-Class到该如何界定、做全球新还是中国新…今天的中国医药业界对创新的理解和选择不尽相同。在臧敬五看来,答案取决于每家公司的定位,看清自己的优劣势,在市场里找到自己的地位非常关键,“没有一个标准说创新药应该怎么做。”
或许一个放之四海皆准的答案并不存在,但天境生物的答案却始终如一。“创立至今,以及到未来,天境生物都会聚焦在创新上,也就是避免同质化”是臧敬五对天境生物创新最精炼的概括。“我们的定位一直是避免同质化,避免跟大家做的完全一样,因为中国从不缺少那样的公司。”
为此,天境生物有着明确的策略,“第一是早动手快推进。我们现在的成熟管线早在2016年刚刚成立时就已经在铺垫了,大家还在做PD-1、PD-L1的时候,天境就开始做CD47、CD73等早期靶点,这些都是今天全球最前沿最有潜力的靶点。”
仅仅早和快是不够的,天境生物的另一个策略是差异化。“定位就是做差异化的创新,因为我们的优势就在这里,从每一个分子中找到创新点和成为创新药的潜力。”
天境生物的整个研发管线按照三波不断创新迭代。2016年成立时天境第一波创新聚焦在CD47、CD73等当时单克隆抗体领域的新靶点上。“中国整个创新发展得特别快,到2017年单抗市场激烈到几乎已经找不到没有人做过的新靶点了。”
无法抢占先发优势的环境里,天境生物顺势转向第二波创新,开始布局双特异性抗体领域。
在双抗上,天境依旧避免同质化,聚焦有差异的产品。包括旨在解决PD-L1单抗耐药性为基础的双特异性抗体,将TJC4 抗体与粒细胞-巨噬细胞集落刺激因子(GM-CSF)结合强化吞噬效应的双特异性抗体。
今年3月,天境生物与ABL Bio合作开发的同时靶向Claudin 18.2和4-1BB的双特异性抗体TJ-CD4B获得FDA批准,成为全球首款、也是迄今为止唯一一款获批临床的Claudin 18.2/4-1BB双特异性抗体,该药物还计划于2021年年内在中国开展相关研究。
“所有的项目在天境如果没有First-in-Class、Best-in-Class的潜力,是不会被立项的。”
天境生物的第三波创新已经开始了。
2021年3月,天境生物分别与两家生物公司达成合作。与比利时Complix的细胞穿膜抗体(CPAB)技术平台合作,开发能够针对膜内靶点的抗体。与上海亲合力生物合作,研发肿瘤局部抗体激活的隐蔽抗体,避免抗体在体内产生副作用。
臧敬五表示:“天境生物的第三波创新将会利用这些革命性的平台来开发创新的‘超级抗体’。”到2021年年底,天境生物预计将建立6~7个这样的新兴生物技术平台合作。
支撑起天境生物一波波创新的是“授权引进”和“自主研发”的双驱动的研发模式,根据“快速概念验证”和“快速产品上市”两条腿走路的战略定位,建立了可快速面向市场的“中国管线”,以及具有突破性潜力的“全球管线”。
臧敬五说:“自主研发对公司来说是战略,是整个公司最重要的部分,而引进对公司来说是战术。战略跟战术的组合在天境生物平衡得很好。三分之二的项目都是自主研发,现不到三分之一是引进项目。
今后天境还是会按照这条路走下去。战略还是自主研发,战术上会在全球找到匹配公司管线的项目或上市产品来增加公司的竞争力。但今后引进不会是大规模的。”
就这样,天境生物将战场一分为二。
授权引进的中国管线在相对较短的时间内快速通过产品打开市场;自主研发的全球管线则在美国及中国开展临床,验证其创新药项目的差异化优势,并寻求国际合作,同时快速推进。多元化的研发方式兼顾创新高度和风险平衡。
一边在创新上攻关,一边用商业来起舞,天境生物的“良性循环”仍在继续。
本文最先刊于《E药经理人》杂志2021年4月刊
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..