▎药明康德内容团队报道
近日,由中国医药工业信息中心主办的《2020年(第37届)全国医药工业信息年会》发布了“2020年中国医药新锐创新力量”榜单。该榜单为今年首次推出,共有10家中国创新医药公司入选。根据公开信息,该榜单评选依据分为产品和企业两个层面,在产品层面考察创新维度、投入维度、技术维度和竞争维度;在企业层面考察特性维度、动力维度、战略维度和发展维度。本文中,我们将梳理这10家公司目前产品管线及最新研究进展。
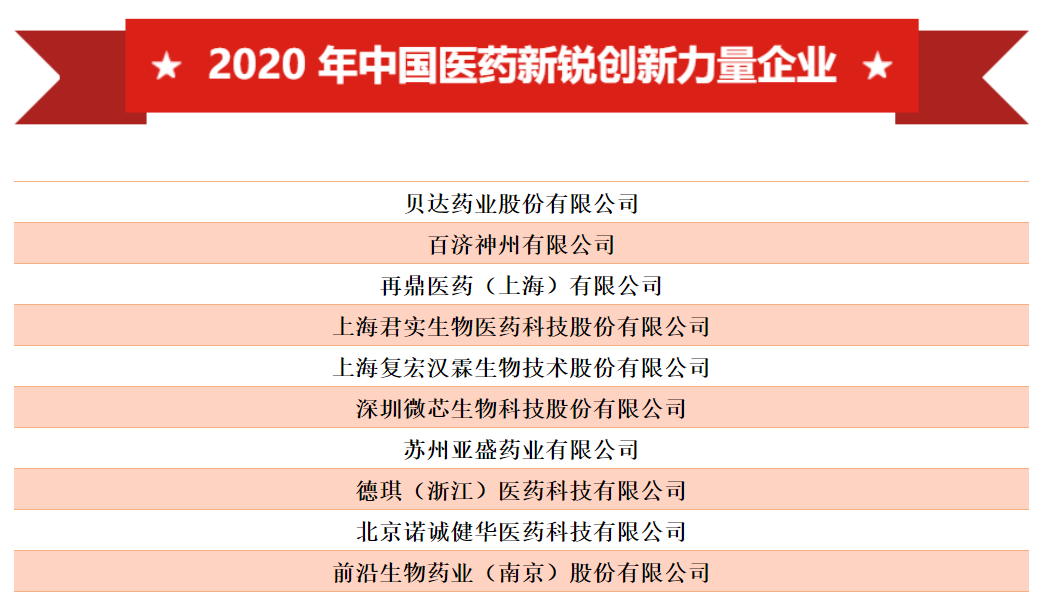
图片来源:参考资料[1]
1、贝达药业
贝达药业成立于2003年,已于2016年在深圳证券交易所挂牌上市。目前,该公司已有1.1类新药盐酸埃克替尼(凯美纳)获批上市。这是一款强效、高选择性的小分子口服表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI),被批准用于非小细胞肺癌的一线治疗。另外,新一代ALK抑制剂恩沙替尼已在中国递交新药上市申请,并被纳入优先审评。
近期,贝达药业迎来多项重要进展。其与天广实生物共同研发的贝伐珠单抗生物类似药(MIL60)已提交上市申请并获受理,由贝达药业与海正生物联合提交;原肌球蛋白受体激酶(TRK)靶向疗法BPI-28592片于近期获得临床试验批准;与美国Agenus公司达成合作,引进后者PD-1抗体balstilimab和CTLA-4抗体zalifrelimab这两款肿瘤免疫单克隆抗体。
2、百济神州
百济神州成立于2010年,已于美国纳斯达克和港交所上市。目前,其已经实现2款自主研发创新药的商业化,分别是BTK抑制剂泽布替尼(zanubrutinib)和PD-1抑制剂替雷利珠单抗(tislelizumab)。另外,该公司拟用于治疗卵巢癌的PARP1/2小分子抑制剂在研产品帕米帕利已在中国递交上市申请,并被纳入优先审评。
根据百济神州2020年第二季度业绩,该公司正在继续推动该公司自主研发早期管线的开发进程,包括BGB-A1217(一款处于1/2期临床开发的TIGIT单克隆抗体)、BGB-11417(一款处于1/2期临床开发的BCL-2抑制剂)、BGB-A445(一款处于1期临床开发的非配位体抗OX40单克隆抗体)、BGB-10188(一款处于1期临床开发的PI3Kδ抑制剂)以及BGB-15025(一款处于临床前开发的HPK1抑制剂)。另外,合作项目中Azymetric™双特异性抗体zanidatamab(ZW25)和在研RAF二聚体抑制剂BGB-3245均在稳步推进中。
同时,该公司还在近期成功完成了一项净收入约为20.7亿美元的注册直接发行;就百奥泰生物的贝伐珠单抗生物类似药(BAT1706)签订了一项在中国的授权、分销、供货协议;并以超5.4亿美元引进Assembly Biosciences公司的三款乙肝治疗在研药物。
3、再鼎医药
再鼎医药成立于2014年,于2017年在美国纳斯达克上市。目前,该公司已在中国成功实现两款产品的商业上市,分别是PARP1/2抑制剂则乐(尼拉帕利)和肿瘤电场治疗产品爱普盾。另外,则乐补充新药申请,以及KIT/PDGFRα激酶抑制剂瑞派替尼(ripretinib)和新型抗生素NUZYRA(甲苯磺酸奥马环素)的新药上市申请,均已获得NMPA优先审评资格。
根据再鼎医药2020上半年公司财报,今年以来,其15项临床研究申请获批(包括CD47抗体ZL-1201),8项临床研究启动。目前,该公司创新产品管线已经包含14个处于临床阶段的管线。另外,该公司还获得Turning Point Therapeutics公司的ROS1/TRK靶向抗癌药repotrectinib在大中华区独家授权,并与再生元(Regeneron)就CD20xCD3双特异性抗体REGN1979达成区域性战略合作。
4、君实生物
君实生物成立于2012年,已于港交所和科创板上市。其自主研发的PD-1抗体特瑞普利单抗已在中国实现商业化,并相继在中国提交两项新适应症上市申请,分别用于复发/转移性鼻咽癌(NPC)和局部进展或转移性尿路上皮癌(UC)患者。同时,该公司阿达木单抗生物类似药UBP1211项目已在中国递交上市申请。另外,其与中国科学院微生物研究所合作开发的新冠病毒中和抗体JS016,正在开展针对轻型/普通型新冠肺炎患者的1b期国际多中心临床研究。
近期,君实生物还达成多项合作。分别有:将获得志道生物授权在全球范围内对IL-2药物(LTC002)开发和商业化的独占许可;将与英派药业成立合资公司,主要从事PARP抑制剂小分子抗肿瘤药物的研发和商业化;与Revitope Oncology等达成研发战略合作,共同研发以双抗原为靶点的“全球新”T细胞嵌合活化癌症疗法。
5、复宏汉霖
复宏汉霖成立于2010年,于2019年在港交所上市。目前,该公司已成功上市了2款产品,分别是首个中国国产生物类似药汉利康(利妥昔单抗)及首个中欧双批的中国国产单抗生物类似药汉曲优(曲妥珠单抗)。另外,该公司阿达木单抗生物类似药HLX03已在中国申报上市,根据公开信息,其有望于今年上市。另外,复宏汉霖正同步就10个产品、8个联合治疗方案于全球范围内开展20多项临床试验。
今年来,复宏汉霖在研管线也迎来新进展。其中,贝伐珠单抗生物类似药HLX04完成3期临床试验,达到主要及次要研究终点;创新型单抗抗DR4抗体HLX56在中国台湾地区获临床试验许可;重组抗CTLA-4全人单克隆抗体注射液HLX13、帕妥珠单抗生物类似药HLX11、地舒单抗生物类似药HLX14等均在中国获批临床。今年5月,该公司还与三优生物、上海之江生物达成项目合作协议,三方将合作研发针对新型冠状病毒肺炎(COVID-19)的全人源抗体药物。
6、微芯生物
微芯生物成立于2001年,专注小分子药物的原创研发。2019年8月,微芯生物在科创板上市,成为了首家通过上海证券交易所科创板注册的医药企业。目前,微芯生物已建立了丰富的产品管线。该公司自主研发的西达本胺是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)口服抑制剂,已在中国获批治疗外周T细胞淋巴瘤、乳腺癌适应症,目前正在弥漫大B细胞淋巴瘤(DLBCL)适应症中开展关键性3期临床试验 。
西达本胺之外,微芯生物产品线中进展最快的是新型胰岛素增敏剂西格列他钠,拟用于2型糖尿病和非酒精性脂肪肝的治疗。2019年9月,微芯生物已在中国提交了西格列他钠治疗2型糖尿病的上市申请,这意味着微芯生物很快将迎来第二款上市产品。此外,微芯生物的产品线中还有靶向AuroaB/VEGFRs/CSF1R三通路的激酶抑制剂、JAK3/JAKS/TBK1选择性激酶抑制剂、PD-1/PD-L1拮抗剂等多种产品,覆盖小细胞肺癌、非酒精性脂肪肝、自身免疫性疾病等多种适应症。其中,JAK3激酶抑制剂CS12192在今年6月获得两项临床默示许可,拟开发治疗类风湿性关节炎。
7、亚盛医药
亚盛医药成立于2009年,致力于开发“first-in-class”与“best-in-class”创新药,已于2019年在港交所上市。在2020年上半年,亚盛医药在新药申报、临床开发、对外合作等多个方面迎来里程碑进展。今年6月,亚盛医药宣布向NMPA递交了第三代BCR-ABL/KIT抑制剂HQP1351的新药上市申请,用于治疗伴有T315I突变的慢性髓性白血病(CML)慢性期和加速期患者,这是亚盛医药创立以来的第一个NDA。
根据亚盛医药新闻稿,2020年上半年该公司研发支出为人民币2.5亿元,进一步推动创新药的研发进展。截至6月30日,亚盛医药已构建包括8个处于临床阶段的小分子候选药物在内的在研产品线,这些在研新药主要专注细胞凋亡路径关键蛋白的抑制剂,通过抑制Bcl-2/Bcl-xL、IAP、MDM2-p53等,重启肿瘤细胞的凋亡程序;以及新一代针对癌症治疗中出现的激酶突变体的抑制剂等。在中国、美国及澳大利亚,亚盛医药有超过40项临床试验正在进行中。除此之外,该公司产品管线还在进一步扩充,包括临床前候选药物Mcl-1抑制剂AS00491、APG-3526,EED抑制剂APG-5918,以及尚处探索阶段的第四代BCR-ABL抑制剂AS1266。
8、德琪医药
德琪医药成立于2016年,是一家专注于创新抗肿瘤药物的生物医药公司,已于近日在港交所递交IPO申请。目前,德琪医药已建立包含12款在研药物的产品管线。其核心产品ATG-010是一种抑制核输出蛋白(XPO1)的SINE化合物,已在美国获批治疗多发性骨髓瘤和弥漫性大B细胞淋巴瘤。目前,德琪医药正在中国就ATG-010进行两项2期注册临床试验,分别用于治疗复发/难治性多发性骨髓瘤、复发/难治性弥漫大B细胞淋巴瘤。
除了ATG-010外,德琪医药还有5款候选药已进入临床试验阶段,分别为:下一代SINE化合物ATG-016、SINE产品ATG-527、ATG-008(第二代口服双靶点的mTORC1/2抑制剂)、ATG-019(一款口服PAK4/NAMPT双靶点抑制剂)、和ATG-017(一款作用于ERK1/2的有效的和有选择的口服抑制剂)。值得一提的是,德琪医药于今年7月刚宣布完成9700万美元C轮融资,并在8月底向港交所递交了IPO申请。
9、诺诚健华
诺诚健华成立于2015年,致力于为全世界正在对抗癌症及免疫系统性疾病的病人提供先进的创新药物,已于2020年3月正式在港交所挂牌上市。成立5年以来,诺诚健华已取得快速发展。目前,该公司已建立丰富的产品管线。其核心产品奥布替尼是一款BTK(布鲁顿氏酪氨酸激酶)抑制剂,已在中国分别提交治疗复发/难治慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)、复发/难治性套细胞淋巴瘤(MCL)两个适应症的上市申请,并被纳入优先审评程序。
此外,该公司的产品线中还包括ICP-192(一款高选择性小分子泛FGFR抑制剂)、ICP-723(一种第二代泛TRK小分子抑制剂)、ICP-105(一种高选择性的FGFR4抑制剂)、ICP-332(一款TYK2靶向药)等多款产品。其中ICP-192正在中国和美国开展多项临床研究,已于近期在中国完成首例尿路上皮癌和首例胆管癌患者入组。ICP-723于今年5月刚在中国获得两项临床试验默示许可,适应症为“拟用于携带NTRK融合基因的晚期或转移性实体瘤的治疗”。
10、前沿生物
前沿生物成立于2013年,已在科创板提交注册申请。该公司自主研发的1类新药艾可宁(艾博韦泰)是一种人类免疫缺陷病毒(HIV-1)融合抑制剂,适用于与其它抗逆转录病毒药物联合使用,治疗经其它多种抗逆转录病毒药物治疗仍有HIV-1病毒复制的HIV-1感染者。艾可宁已于2018年5月在中国获批上市,根据新闻稿,这是全球首个长效HIV-1融合抑制剂。
除了艾可宁,前沿生物目前还有两款在研产品。一款是“艾可宁+3BNC117联合疗法”。根据前沿生物公告,3BNC117是一种广谱中和型抗体(bNAb),不仅能够和其他抗艾药物一样抑制HIV病毒复制,而且可以介导针对HIV病毒和被感染细胞的免疫应答。将艾可宁与3BNC117联合使用,旨在利用两个分子的不同抗病毒机制,最大程度抑制不同流行的HIV病毒包括耐药病毒。2019年5月,该联合疗法已获得NMPA批准直接进入2期临床。2019年11月,美国FDA已授予该联合疗法快速通道资格,用于治疗MDR(HIV多重耐药)。
另一款在研新药是AB001。AB001是一种新型的透皮贴片处方型镇痛剂,可用于治疗源自于骨骼、肌肉和关节等不同部位的急慢性疼痛。作为一种第三代贴剂产品,它的非水凝胶剂型适用于各种类型的皮肤,药物透皮能力强且组织渗透性高,能在病灶部位有效拮抗发炎和缓解疼痛。
祝贺这10家公司入选“2020年中国医药新锐创新力量”榜单!希望这些公司能够持续带来创新产品,造福更多患者。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..