VIR-2218是一款正在开发用于功能性治愈慢性乙型肝炎病毒感染的核糖核酸干扰(RNAi)治疗药物。 VIR-2218增强了在体内效力所需的代谢稳定性,同时降低了序列匹配的脱靶效应。 VIR-2218旨在沉默所有10种HBV基因型的cccDNA和整合DNA中的所有HBV转录物。在本界欧洲肝病学会年会(EASL2020)上,研究人员提供了VIR-2218在慢乙肝患者中进行的Phase 2期试验的中期安全性和抗病毒活性数据。
研究纳入了接受核苷酸逆转录酶抑制剂治疗且无明显纤维化/肝硬化的HBeAg阳性或HBeAg 阴性病毒抑制慢乙肝患者作为受试这,在第1天(第0周)和第29天(第4周)接受了2剂量的VIR-2218皮下注射或安慰剂治疗。四组HBeAg阴性受试者分别接受20mg、50mg、100mg或200 mg;50mg和100mg剂量组增加了两个队列。两个队列的HBeAg 阳性受试者接受50mg或200 mg。每个队列包括4名受试者,按3:1的比例随机接受VIR-2218或安慰剂。评估包括安全性和所有患者进行第二剂用药后12周随访的HBsAg水平,对达到预定HBsAg下降目标的患者进行另外32周的随访。
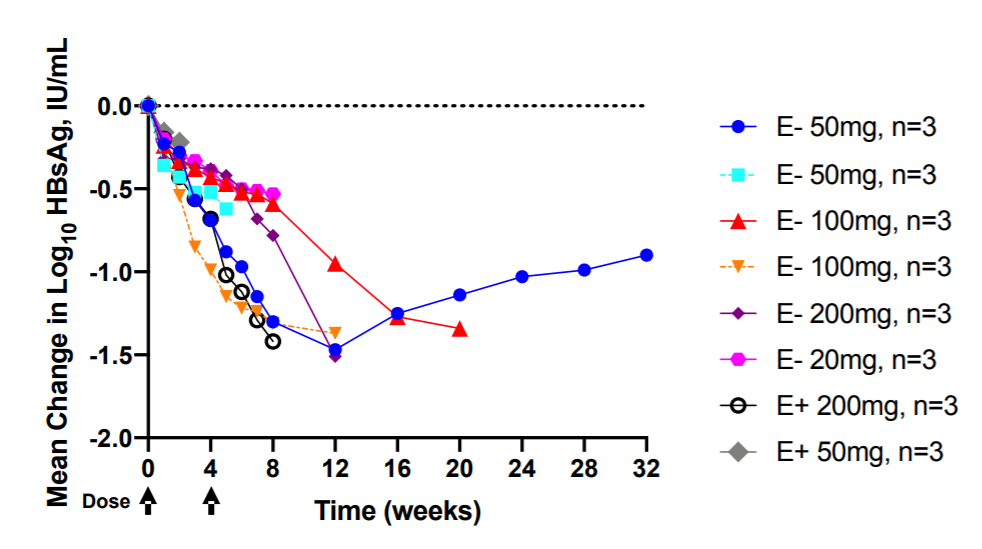
在这项正在进行的试验中,已经有24名慢乙肝患者接受了VIR-2218用药,并且处于不同的随访阶段。没有患者因不良事件(AE)而停药,大多数治疗中出现的AEs的病情轻。没有观察到临床上明显的ALT升高。
剂量为50 mg的部分患者在第12周时已达到HBsAg水平的最大下降,在接受VIR-2218治疗的患者中,平均下降了1.5 log10。值得注意的是,该队列经过28周了仍一直保持着 HBsAg 平均下降1.0 log10。在其他人群中,HBsAg 继续下降,至少观察到两种模式:早期应答和延迟应答。
综上数据,研究认为,慢乙肝患者对两个月剂量的 20 mg - 200 mg VIR-2218 耐受良好。在HBeAg阴性和HBeAg 阳性患者中以及在所有剂量水平下均观察到HBsAg的大量降低。下降的差异模式表明,HBsAg 的早期应答(<8周)可能无法预测下降的最终幅度。在慢乙肝患者中对VIR-2218进行的评估仍在进行中。
信息来源EASL2020AS068
Preliminary safety and antiviral activity of VIR-2218, an Xtargeting HBV RNAi therapeutic, in chronic hepatitis B patients
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..