与国际药厂达成License-out协议不仅是创新药企业实力的重要体现,更是自主创新药进入国际市场的重要渠道。
4月20日,恒瑞医药的PD-1卡瑞利珠单抗License-out的消息再次引起业界对这种方式的关注。自2017年中国药监局加入ICH以来,国产创新药License-out的案例越来越多。
据E药经理人不完全统计,2019年以来披露的License-out案例至少有12起,多为近几年兴起的生物新贵公司,产品集中在肿瘤免疫领域。而被授权方不仅仅是国际大药企,还出现了日本、韩国等中型生物制药公司,复宏汉霖还尝试将产品引进到一带一路国家;而具体形式在传统的产品License-out之外也出现了技术授权等更加先进的方式。中国自主创新药出海形式正在越来越丰富和多样化。
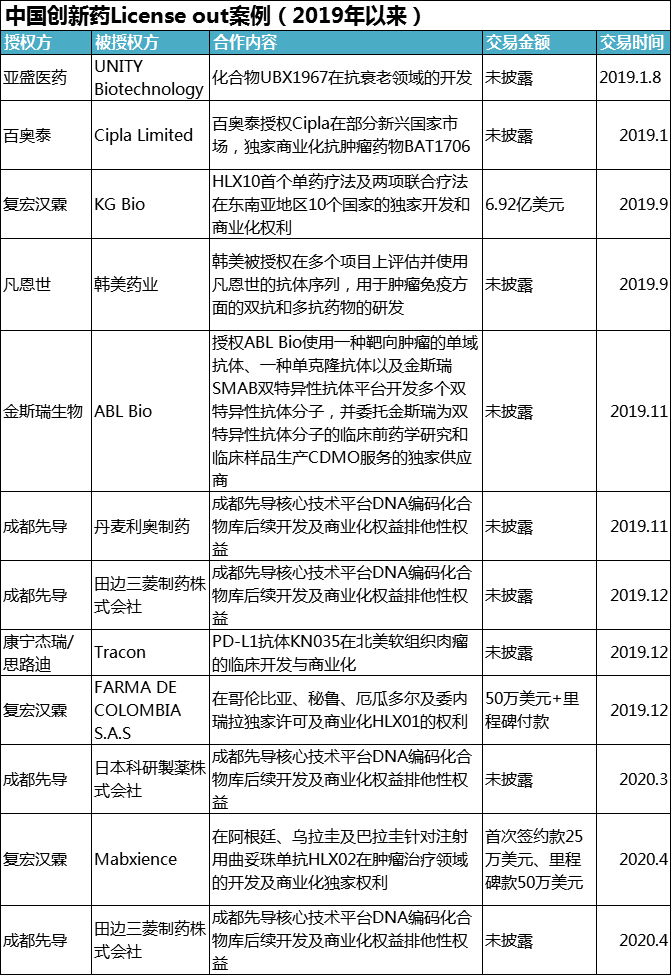
资料来源:E药经理人统计
01 恒瑞PD-1再出海,国产PD-1冲刺国际市场
2015年9月,恒瑞医药以2500万美元首付款加总额可达7.7亿美元,将具有自主知识产权的PD-1抗体SHR-1210国外权益出售给美国Incyte公司,实现了中国企业第一次对外转让创新生物药品。
但2018年2月,恒瑞医药与Incyte合作开发PD-1抗体的协议最终终止。收回海外权益后,恒瑞医药决定自主推动包括美国在内的国际多中心临床试验。
而2020年4月20日,卡瑞利珠单抗再次海外授权。恒瑞医药与韩国CrystalGenomics(CG)公司达成8775万美元的协议。CG将获得恒瑞医药的PD-1抗体注射用卡瑞利珠单抗在韩国的独家临床开发、注册和市场销售的权利,可进行研发和销售卡瑞利珠单抗用于所有人类疾病。
值得注意的是,在本次合作中,恒瑞医药还宣布与CG公司设立联合管理委员会,对许可产品的开发和市场营销进行战略监管。联合管理委员会由恒瑞的 3 名代表和 CG 公司的 3 名代表组成。除非根据双方约定提前终止,该协议将持续到销售提成期结束。不难猜测,这也许是恒瑞医药经历了与Incyte合作终止,再次海外授权时所做的应对之策。
PD-1/L1抗体作为近几年最热门的产品,也是国产创新药进行海外授权的热门品种。比如2017年百济神州授权新基PD-1单抗替雷利珠单抗在亚洲地区(除日本)以外的实体瘤开发权益,交易总额达13.93亿美元,也创造了当时交易金额最高的License out项目。后来由于BMS收购新基,百济神州将PD-1全球开发权收回自己手中。
2019年12月,康宁杰瑞与思路迪联合开发的PD-L1单抗KN035授权TRACON在以美国为主的北美市场进行治疗软组织肉瘤的临床开发和商业化。KN035被认为有望成为全球首个可皮下注射给药的PD-L1肿瘤免疫治疗药物。
随着中国PD-1/L1第一梯队已经形成,在研竞争项目也愈加激烈,国内市场已经由蓝海变成红海。PD-1/L1开始将眼光瞄准海外更大的市场,一方面能获得更多的收益,一方面也能证明产品本身的品质,有利于在激烈的同类竞争中为自己增添筹码。
02 “出海”新目标:一带一路国家
2020年3月31日,复宏汉霖宣布与生物技术公司Mabxience达成独家许可协议,授予其在阿根廷、乌拉圭及巴拉圭针对注射用曲妥珠单抗HLX02在肿瘤治疗领域的开发及商业化独家权利。
HLX02是复宏汉霖的重磅品种,其与原研开展了“头对头”国际多中心(中国大陆、乌克兰、波兰和菲律宾)3期临床试验,且中欧双报。2019年6月,HLX02成为中国首个在欧盟报产并获得受理的“中国籍”生物类似药。
对于该产品,复宏汉霖早已开展了国际商业化布局,包括授予英国全球性制药公司Accord Healthcare在欧洲、中东、北非地区和部分独联体国家共计70余个国家的独家商业化权利;授予知名制药企业Cipla在亚太和拉丁美洲地区部分新兴国家市场的开发和商业化权利;授予总部位于中国香港的雅各臣药业在中国香港及中国澳门的独家商业化权利。
国内曲妥珠单抗生物类似药竞争激烈,包括海正、正大天晴、嘉和生物等都在布局,原研产品赫赛汀也已经通过降价进入国家医保目录。欧美国家市场,生物类似药的竞争也同样激烈。但与此同时,南美洲发展中国家对于高质量的用药需求还未得到满足,复宏汉霖开辟性地将高质量生物类似药推向这些国家,大大加快了产品的国际化进程,同时提升销售收益。
除了HLX02,复宏汉霖自主研发的创新生物药PD-1单抗HLX10也在东南亚新兴市场进行许可授权。2019年9月,复宏汉霖授权印度尼西亚制药公司KG Bio进行HLX10首个单药疗法及两项联合疗法在东南亚地区10个国家的独家开发和商业化权利。
与国内PD-1市场激烈的竞争格局不同,东南亚市场鲜见本土及国外的PD-1药物。而复宏汉霖正是看到了这个潜在的蓝海市场,于是选择了这一充满机遇的区域作为其PD-1产品HLX10海外授权的首站。
此外,不同于2018年之前,国产创新药License-out对象多集中在跨国药企巨头,近两年交易对象中出现了日本、韩国等国家的中小型生物制药企业。比如成都先导与日本田边三菱株式会社、利奥制药、日本科研制药达成相关转让协议,金斯瑞与韩国生物技术公司ABL Bio签署协议,凡恩世与韩国韩美药业达成授权许可协议,都代表着国产创新药在出海深度、广度上有了质的提升。
03 从产品授权到技术授权
纵观国产创新药License-out历史,2019年之前,这种合作协议更多是产品销售权益方面的授权,而2019年以来,出现了更丰富的形式。
2019年11月,金斯瑞生物与韩国生物技术公司ABL Bio签署协议,金斯瑞将授权ABL Bio使用一种靶向肿瘤的单域抗体、一种单克隆抗体以及金斯瑞SMAB(Single-Domain Antibody fused to Monoclonal Ab) 双特异性抗体平台开发多个双特异性抗体分子,并委托金斯瑞为双特异性抗体分子的临床前药学研究和临床样品生产CDMO服务的独家供应商,加速肿瘤免疫抗体创新药物的开发。
据介绍,金斯瑞的SMAB平台突破了传统双抗平台免疫原性风险高、成药性差、规模化生产难的诸多壁垒,开发过程高效。ABL Bio Inc. 是一家专注肿瘤免疫和神经退行性疾病抗体疗法开发的韩国生物技术公司,正在积极开发多个围绕4-1BB靶点的双特异性抗体和多个基于双特异性抗体的全球首创和同类最佳免疫疗法。
随着新药开发难度越来越高,新药研发相关技术平台已经成为各大药企的竞争壁垒所在。成都先导为小分子新药发现建立了一个以DNA编码化合物库的设计、合成和筛选为核心的技术平台,已经完成千亿级结构全新、具有多样性和类药性DNA编码化合物的合成。正是依靠该技术平台,成都先导先后与武田制药、丹麦利奥制药、田边三菱制药株式会社、日本科研制药株式会社等达成了多份产品转让协议,在License-out方面收获满满。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..