摘要
abstract
1月CDE共承办药品注册申请648件
79个一致性评价品种获CDE承办,其中16个品种为首家申报
8个品种有首家企业提交仿制申请
11个新注册分类仿制药获批
21个品种有企业通过一致性评价
7家企业的新型冠状病毒检测产品获应急审批
CDE总体承办情况
据MED中国药品审评数据库2.0统计,2020年1月CDE共承办药品注册申请648个。除新药申请和进口申请外,仿制申请和一致性评价申请比上月均有所上升。
2019年7月-2020年1月CDE承办药品注册申请情况(按受理号计)
一致性评价补充申请承办情况
1月有79个药品的一致性评价补充申请获CDE承办(2019年12月为66个),其中口服制剂有49个,注射剂有30个,有16个品种为首家企业开始一致性评价。详细情况请见下表:
2020年1月CDE补充申请(一致性评价)口服制剂品种承办情况
2020年1月CDE补充申请(一致性评价)注射剂品种承办情况
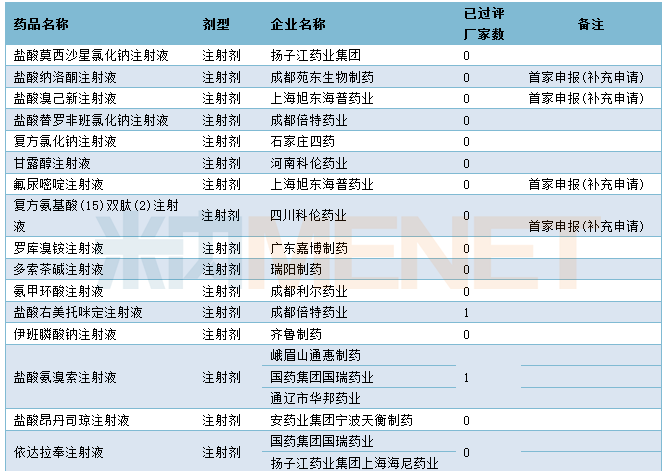
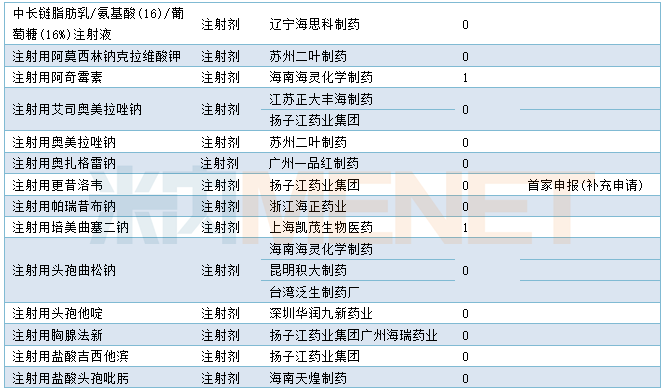
(说明:仅统计以补充申请申报的一致性评价受理号,过评情况按药品名称统计)
新药申请承办情况
1月有45个药品的新药申请获CDE承办,其中属于1类新药的有34个,2类改良型新药3个,6.1类中药新药2个。详细情况请见下表:
2020年1月国内新药申请承办情况
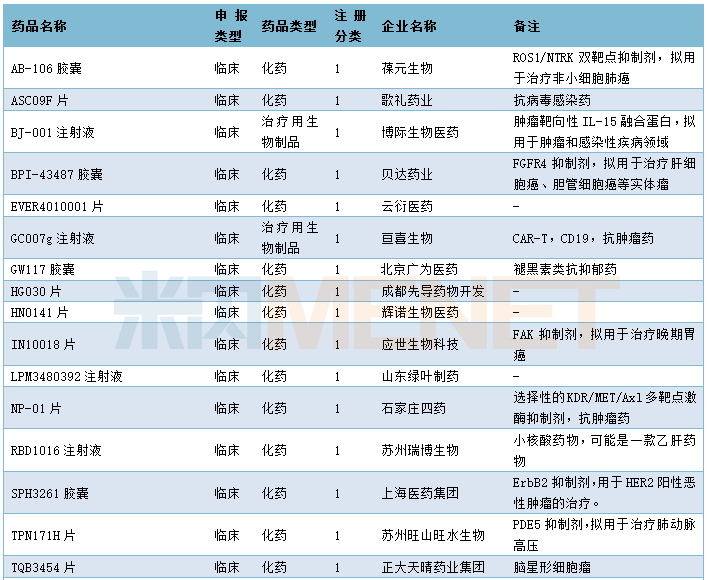
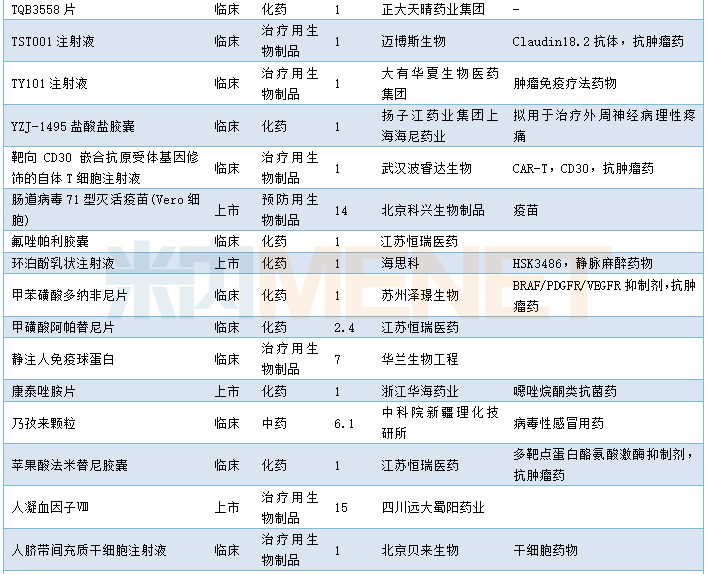
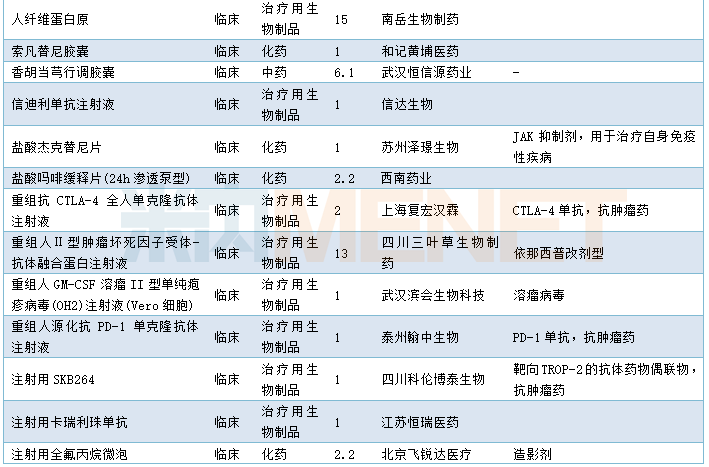
仿制申请承办情况
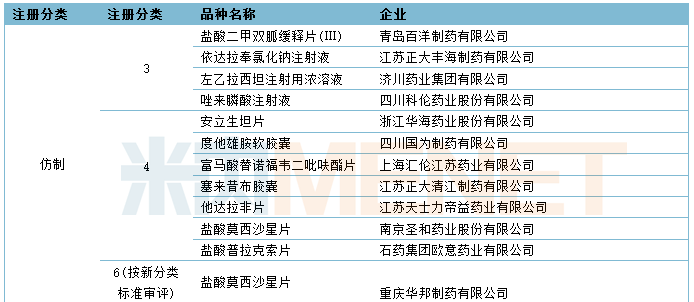
1月CDE共承办57个品种的仿制申请,其中按3类申报的品种有13个,按4类申报的品种有44个,19个品种目前已有企业通过或视同通过一致性评价,8个品种为首家企业提交仿制申请,详细情况请见下表:
2020年1月国产仿制申请承办情况
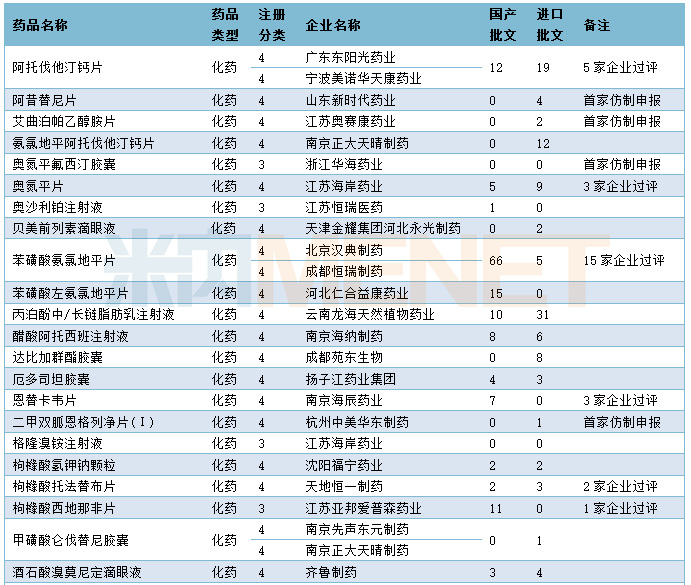
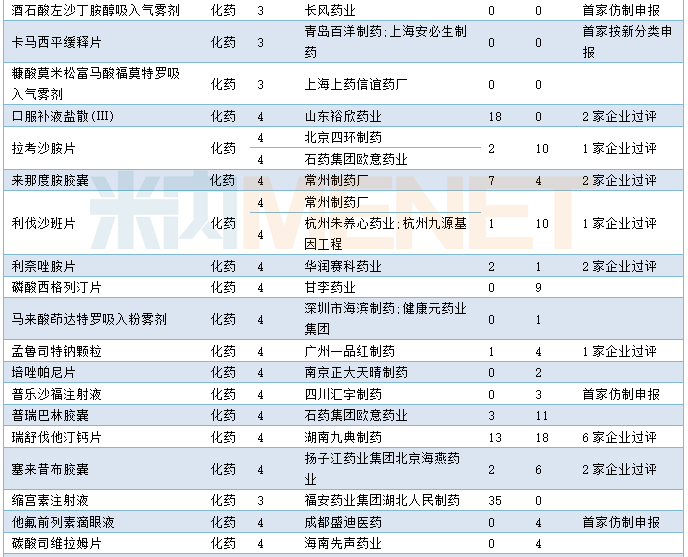
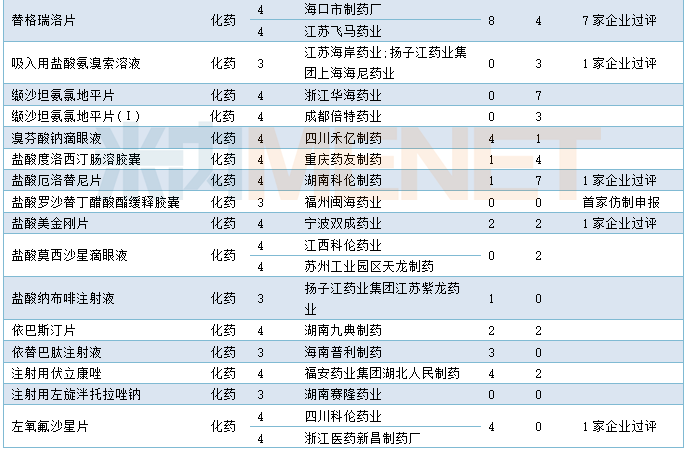
进口申请承办情况
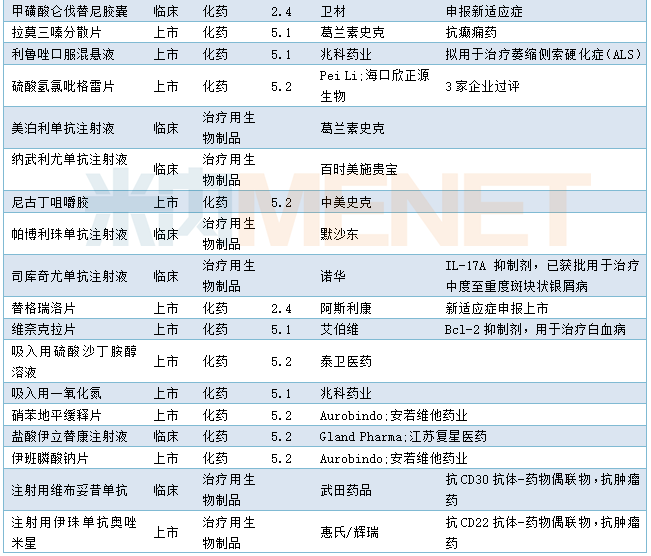
1月CDE共承办31个药物的进口申请,其中1类新药有2个,2类改良型新药有3个,5.1类进口原研药6个,5.2类进口仿制药9个。具体情况请见下表:
2020年1月进口申请承办情况

审批情况
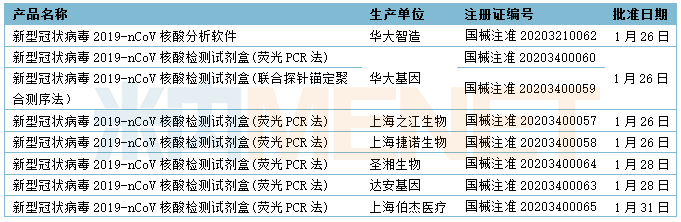
1月有多个仿制药以及一致性评价品种获批。此外,为遏制新型冠状病毒疫情蔓延,国家药品监督管理局根据《医疗器械应急审批程序》应急审批多家企业的新型冠状病毒检测产品,截至1月31日,已有7家企业的新型冠状病毒检测产品获应急审批,具体情况请见下表:
2020年1月部分品种获批情况

(说明:按企业公告或相关报道统计获批时间)
新型冠状病毒检测产品应急审批情况
数据来源:米内网MED药品审评数据库2.0、CDE、NMPA;相关统计截至2020年1月31日,统计字段按药品名称统计。
本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..