很明显,这一指导文件的发布既是对各方的推动,同时也是巨大的挑战。同样一份文件,对于监管层、申办方、临床服务机构以及医院端来说,其代表的含义也不尽相同。如何使这样一个政策更好的成为药品审评审批的补充,提高现实可操作性,可能是接下来需要关注的重点。
1月7日,国家药监局把2020年的一号文件,留给了此前就备受行业关注的真实世界证据支持药物研发与审评。
在其官网上,药监局同时公布了《真实世界证据支持药物研发与审评指导原则(试行)》,以及该文件的起草说明。作为国内发布的首个真实世界证据支持药物研发与审评的指导文件,这被视为新药研发审评道路上的里程碑事件,并迅速引起了行业的密切关注。
事实上,如何利用真实世界证据评价药物的有效性和安全性,早已经成为国内外药物研发和监管决策中日益关注的热点问题。这是基于一个行业现状,即随机对照临床试验(RCT)虽然被认为是评价药物安全性和有效性的金标准,但其研究结论外推于临床实际应用时可能会面临挑战,或者存在传统的药物临床试验可能难以实施或需高昂的时间成本等问题。关于真实世界证据的研究也就应运而生。
这一点国外进行的显然更早。2016年12月,美国颁布《21世纪治愈法案》,要求FDA在医疗产品审评和监管程序中纳入真实世界证据(Real-World Evidence, RWE),而自此之后,美国市场也已有产品借此而获批,例如去年辉瑞的乳腺癌药物爱博新基于真实世界证据而被获批用于男性乳腺癌治便被认为是目前真实世界证据在药品研发上市中代表性的案例。
而中国则是在2018年8月,吴阶平医学基金会和中国胸部肿瘤研究协作组发布了《2018年中国真实世界研究指南》。国家药监局正式启动相关指导原则的起草工作则是在2018年的11月,经数次研讨后,2019年5月,CDE发布了《真实世界证据支持药物研发的基本考虑》(意见稿),于2019年5—8月广泛征求意见,并收到千余条反馈意见。在此基础上,《真实世界证据支持药物研发与审评的指导原则(试行)》才正式形成。
01 何为真实世界研究?
真实世界研究是指针对预设的临床问题,在真实世界环境下收集与研究对象健康有关的数据(真实世界数据)或基于这些数据衍生的汇总数据,通过分析,获得药物的使用情况及潜在获益-风险的临床证据(真实世界证据)的研究过程。
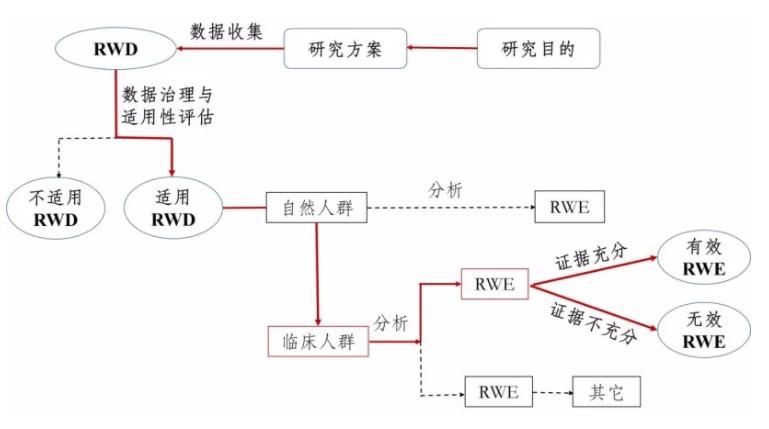
与真实世界证据对应的是随机对照试验(RCT),RCT一般被认为是评价药物安全性和有效性的金标准,并为药物临床研究普遍采用。曾经一位专家举了个生动的例子来描述RWS与传统RCT的关系:RCT是在一个理想状态下钓鱼,比如一个鱼塘或者一个网箱,这是一个高度控制的人工环境;而真实世界研究是在现实中钓鱼,是真实的江河湖泊,这是自然环境。
02 这些领域将显着受益
之所以一经发布便引发行业密切关注,很大程度上在于关于真实世界证据的研究,将在很大程度上给接下来药物的研发、审评以及药物的监管政策带来新的思路。
具体来说,《指导原则》已经对对真实世界证据支持药物监管决策给出了几项应用范围,具体如下:
(一)为新药注册上市提供有效性和安全性的证据;
(二)为已上市药物的说明书变更提供证据;
(三)为药物上市后要求或再评价提供证据;
(四)名老中医经验方、中药医疗机构制剂的人用经验总结与临床研发。
显而易见,该指导原则对中药来说有非凡的意义。对于中药,用观察性研究代替一期二期研究,提出研发路径,弥补历史数据的缺失。
在业内人士看来,在中药注射剂等在临床面临存在安全性信息有限、疗效结论外推不确定、用药方案未必最优、经济学效益缺乏等不足的挑战之时,利用真实世界数据进行更全面的评估,可以得到充分的临床证据。
实际上,在此前还处于RWS(真实世界研究)阶段时,已经有相当多的国内中药企业开始了相关的尝试。例如,2015年贵州益佰制药推动的全球首个抗肿瘤药艾迪注射液的10万例真实世界临床研究启动;2016年12月,安徽九方制药的葛酮通络胶囊10万例真实世界研究项目启动;以及翔宇药业的蒲苓盆炎康颗粒、上海和黄药业的生脉注射液、步长制药的脑心通胶囊等均开展了RWS项目。
另一个直接受益的领域为医疗大数据。作为国内较早探索开展RWS的医疗大数据公司,以及指导原则的参与方,零氪科技首席运营官罗立刚对E药经理人透露,其实从征求意见稿发布以来,零氪已有一些case在往前走了,主要是药品上市后扩适应症的真实世界研究,包括进口药,也有国内创新药。
从数据上来看,来自中国的研究登记逐年上升。据ClinicalTrials数据不完全统计,以“Real world”相关关键词登记在册的研究达到 1700 多项,其中来自中国的研究登记超过180 项,涉及肿瘤、心血管、内分泌、肝病和不良药物事件等多个领域。且据该数据研究完成时间预计2018—2022年将出现真实世界研究结论发布的井喷。
03 这四点思考仍值得关注
为探究该文件的意义,E药经理人也在第一时间采访到业内具有多年真实世界研究和大数据管理的专家。基于过往的经验,专家分享了四点体会:
第一,指导原则虽然是试行版,但基本上明确了国家对基于数据库、大数据来源的真实世界证据在药物审评审批中的作用和使用指导:包括如何合法合规使用数据,在哪些方面是鼓励支持的,为医疗大数据从业者指明了方向。
第二,实际操作层面仍有很长的路要走。主要原因在于大家对于指导原则的理解和接受度不同,每个团队在各自项目运用上或有差异;除此之外,目前在RWE层面,可以使用的成熟数据库和大数据的基础比较薄弱。指导原则中着重提出了对数据质量的要求,需要我们重视来自数据端的潜在风险。另外,面对庞杂的大数据,用什么方法来保证数据的完整性和相关性,以及结果的可靠性,也是需要在实践中不断总结和提高的部分。这些工作并不是任何一家科研机构或是一家企业就能单独完成的,需要整个行业群策群力。
第三,这一指导文件的发布既是对各方的推动,同时也提出了挑战。对于申办方来说,是运用真实世界研究,还是RCT研究,对资源和方法的把握将提出更高的要求;对于包括CRO在内的临床服务机构来说,还有很多机构达不到指导原则中提出的能力要求。未来可能出现少数几个CRO,或者说一种更新的形式去进行资源整合。对于医院和公共资源的数据端来说,也是极大挑战,是否能够合规开放、如何开放、如何有效共享医疗数据,如何达到数据的一致性,从而提供完整有效的真实世界证据来支持药物的审评审批,都是亟待解决的问题。
第四,该原则将成为以医疗大数据为主导的医疗技术创新的重要指导性文件。各方需要真正重视起来、行动起来,协作努力推动我国卫生信息系统、医保信息系统、不良反应监测系统和专病队列数据库等的建设和进一步完善,用好管好医疗大数据,解决未满足的治疗需求,造福人民。
总体来说,指导原则既体现了与国际标准的对接,又对行业参与的各方提出了明确的要求和未来的发展方向。这个指导原则的出台在短期会加速罕见病和某些儿科用药的审评审评进程,长期来看会逐步影响临床数据采集和分析评估方式,推动临床证据积累和治疗方案的优化。真实世界证据也会在药物审评中越来越受到重视,发挥RCT研究不能替代的作用。
此前也有业内专家表示:真实世界研究不应被过分炒作,它是一种与随机对照临床试验差异发展、互为补充的一种研究方式或理念,即让受试者尽可能在“临床上该怎么治就怎么治”的状态下,进入观察、分析的研究方式。因为RCT的优势是通过控制偏倚和混杂,利用较少病例在较短时间内获得疗效和安全性数据,这些方面RWS很难满足。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..