为了加快仿制药上市,FDA在1984年颁布了《药品价格竞争和专利期恢复法案》(Drug Price Competition and Patent Term Restoration Act),也就是著名的Hatch-Waxman 法案,提供了一种仿制药在原研专利保护到期之前上市的可能性。
该法案鼓励仿制药企业对原研药的市场独占发起挑战,规定了仿制药简略新药申请(ANDA)材料中需要作出专利声明的几种情况,其中第IV种情况(P IV)是仿制药申请人声明FDA橙皮书所列的某个原研药的专利无效,或者申请人提交申请的仿制药的生产、使用、销售不会侵犯该原研药的专利,也就是P IV专利挑战。首个发起P IV专利挑战并成功上市的ANDA仿制药,可以获得180天市场独占期。
FDA一直致力于提高与仿制药申请人的沟通效率,特别是在仿制药厂商提交简略新药申请ANDA之前,FDA希望有尽可能充分的信息给申请人参考。因此FDA在其网站会及时公布仿制药企业发起的适应性请愿(uitability petitions),以及P IV专利挑战案例(Paragraph IV Patent Certifications List)。
此前,P IV专利挑战案例提供的信息非常有限,只有药品名字(剂型、规格)以及第一个包含有P IV挑战声明的完整ANDA的提交日期。不过经常就会漏掉比这个ANDA更早的有可能获得180天独占期的仿制药申请。
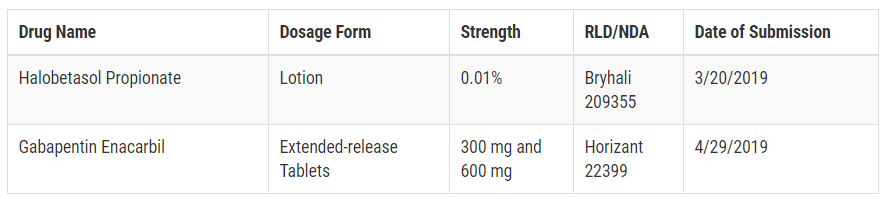
现在,FDA网站上的P IV专利挑战案例有了更丰富的信息,包括针对同一原研药的首仿ANDA数量,针对具体仿制药的180天市场独占期的授予状态,首次批准日期、上市状态,原研专利的到期时间等。这些信息可以为仿制药厂家的决策提供更全面的参考。
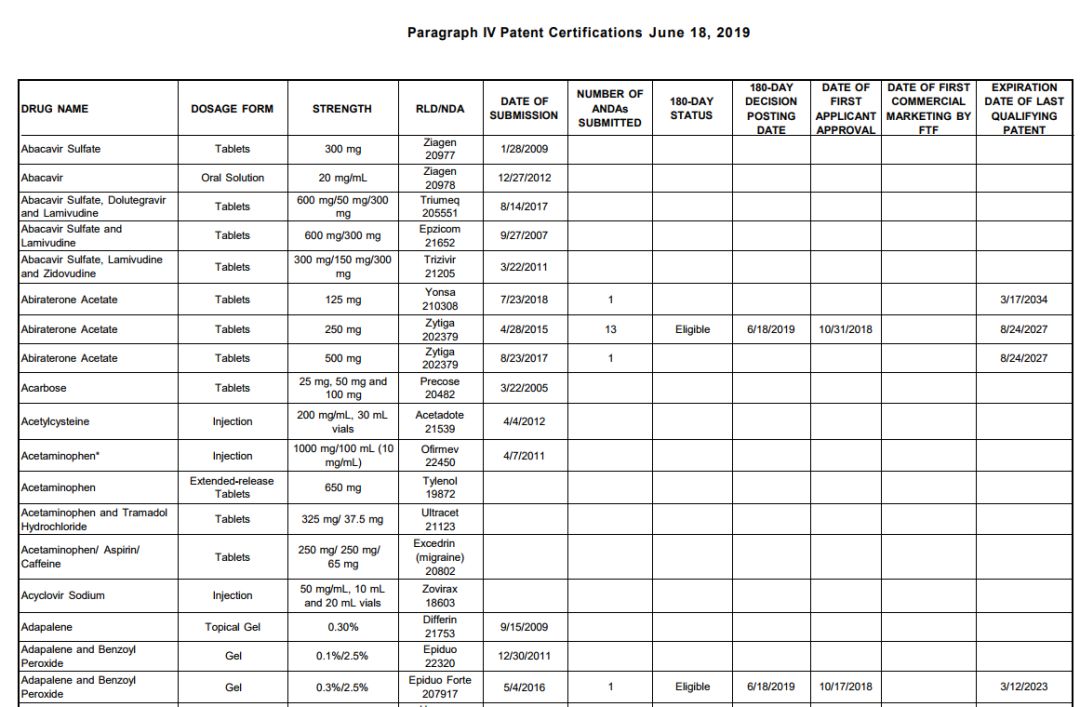
在美国的仿制药市场竞争制度设计下,180天的市场独占期非常关键。仿制药企业都会抢着新药上市满4年的那一天提交包含P IV挑战声明的ANDA申请,以独享或共享这180天市场独占期。如果不发起P IV专利挑战,只能等新药上市过了5年的数据保护期之后才能提交ANDA,那个时候市场基本已经被首仿和原研瓜分殆尽,市场机会就很有限了。
FDA官员表示:这些公开数据将提高公众可掌握信息的透明度,比如某个品种的ANDA已经获得了180天市场独占资格,但仿制药申请人可能出于其他原因并未在市场上进行销售。此外,我们这次公开的信息还包括了潜在的可以共享180天市场独占期的ANDA数量,这个数据其实是一个信号,提示其他仿制药企业还要不要再立项开发这个品种。从6月18日开始,此后包含P IV专利挑战的ANDA信息都会被FDA有更充分的公开。
FDA此次公开更多的P IV专利挑战案例信息,体现了FDA对药品市场竞争方面的关注度。仿制药企业会根据“首仿”ANDA的数量来调整自己的仿制药立项决策,比如看到某个品种的首仿ANDA不如自己想想的那么多,就会抓紧时间在180天后更早一点进行ANDA申报。
此外,FDA在打击原研药企业恶意阻遏仿制药竞争方面也采取了行动,公布了一系列拒绝仿制药企业购买其产品作为参比制剂的原研药公司名单,发布了无竞争的过专利期原研药清单,并加快该清单上申请人少于3家的ANDA等等。这些行动的退出,也都是FDA前局长Scott Gottlieb的功劳。
相关阅读:
还“怼”生物类似药吗?FDA局长发推批评原研厂商
突发:FDA局长Scott Gottlieb宣布退休
狙击高药价!FDA局长呼吁增加海外药品进口
据了解,FDA另外一份比较实用的行业指南很快就会出台,就是将仿制药的最终批准(final approval)转变为暂定批准(tentative approval)。
这份指南旨在帮助仿制药企业解决一种比较少见的现实问题。有时候,尽管一个ANDA已经获得FDA的完全批准并上市,但是由于不可完全预期的专利侵权问题,法院在审理专利诉讼时会要求先终止该仿制药的上市资格,以避免对原研专利的侵害。但是FDA之前的工作程序里面并没有关于如何处理这种上市后可能造成专利侵害的情况说明,也没有关于如何将一个ANDA从最终批准转换为暂定批准的操作说明。FDA此份指南将帮助解决这个政策瑕疵问题。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..