1月17日,国务院办公厅正式发布了《国家组织药品集中采购和使用试点方案的通知》,再次明确了选择原定的11个城市,从通过质量和疗效一致性评价的仿制药对应的通用名药品中遴选试点品种,由国家组织药品集中采购和使用试点。可见,一致性评价+带量采购将会成为2019年医药界的主旋律,且比2018年更加热闹,竞争更加激烈。
截至2019年1月18日,通过(或视同通过)一致性评价的品规数为173个,涉及产品87个。在一众企业中,科伦作为输液龙头交出来6个产品过评的成绩单,实在亮眼。最近几年,受限抗限输影响,科伦一直谋求转型,在保持输液领域的绝对领先地位的前提下,构建“以仿制推动创新,以创新驱动未来”的产品线战略布局,接下来这家企业又将有哪些新气象呢?
华丽转型:稳固输液龙头地位,非输液业务增长迅速
图1:2014-2018年科伦药业营收情况(单位:亿元)
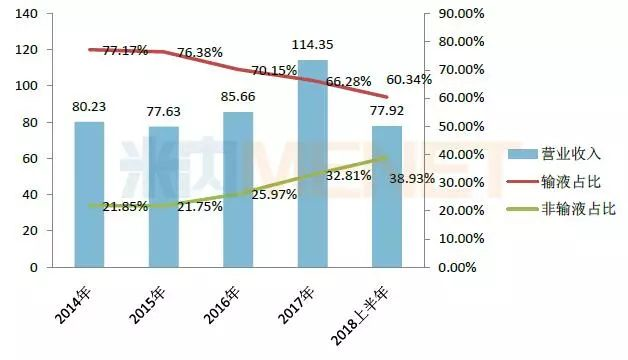
(来源:上市公司年报)
科伦药业年报中提到,在限制门诊输液、控制抗生素规范使用、分级诊疗/双向转诊还处于政策执行期等因素影响下,整个输液市场的总容量有小幅度缩减。在价格控制、招标降价的背景下,公司输液和非输液产品整体销量未受明显影响,公司利用市场整合契机,加大了市场投入,持续优化产品结构,降低生产成本。
在输液领域,公司继续推进产品软塑化进程,调整产品结构,扩大了软塑产品销售,高毛利软塑产品销售结构占比进一步提升,产品结构的优化增加了公司利润贡献,生产成本降低,增加毛利贡献。在非输液领域,公司在非输液制剂和抗生素板块,通过加大市场投入,推进终端市场销售。
2018年,科伦药业预计归属于上市公司股东的净利润盈利为11.60亿~13.85亿元,同比增长55%~85%。业绩增长原因是公司输液产品结构持续优化,加强销售推广力度,直销客户增加,毛利额和毛利率增长;伊犁川宁产能释放,全面达产,利润增加等。
6大产品已通过一致性评价,3个为首家通过
2018年,我国医疗体制改革继续深入推进,国家医药政策一方面鼓励创新,另一方面推进上市仿制药的质量与一致性评价,促进医药企业提质增效,以新技术、新业态、新模式推动产业变革与发展。截至目前,科伦药业已有6大产品通过了一致性评价,其中氢溴酸西酞普兰片、甲硝唑片、替硝唑片为首家通过。
表1:科伦药业已通过一致性评价产品情况
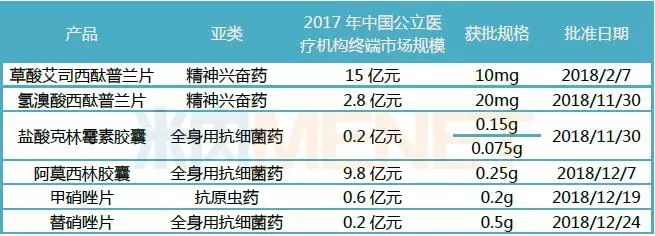
(来源:米内网MED中国药品审评数据库2.0)
氢溴酸西酞普兰片的适应症为抑郁性精神障碍(内源性及非内源性抑郁)。据米内网数据显示,2017年在中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端,氢溴酸西酞普兰片的销售额为2.8亿元,领军企业灵北占72.29%的市场份额,TOP2企业四川科伦药业占12.56%。科伦药业为该产品首家通过一致性评价的企业,目前尚无其他企业提交一致性评价补充申请,人福普克药业(武汉)以及西南药业已完成BE。
甲硝唑片用于治疗肠道和肠外阿米巴病(如阿米巴肝脓肿、胸膜阿米巴病等),还可用于治疗阴道滴虫病、小袋虫病、麦地那龙线虫感染等,目前还广泛用于厌氧菌感染的治疗。据米内网数据显示,2017年在中国公立医疗机构终端,甲硝唑片的销售额为6126万元,领军企业山东齐都药业占18.45%。科伦药业为该产品首家通过一致性评价的企业,目前华中药业、宜昌人福药业、江苏悦兴药业等6家企业的一致性评价补充申请正在审评审批中。
替硝唑片用于各种厌氧菌感染,也可用于结肠直肠手术、妇产科手术及口腔手术等的术前预防用药,也可作为甲硝唑的替代药用于幽门螺杆菌所致的胃窦炎及消化性溃疡的治疗。据米内网数据显示,2017年在中国公立医疗机构终端,替硝唑片的销售额为2360万元,领军企业鲁抗医药赛特占27.58%。科伦药业为该产品首家通过一致性评价的企业,目前丽珠集团丽珠制药厂的一致性评价补充申请正在审评审批中。
16个产品一致性评价在审,9个注射剂中有3个为十亿品种
表2:科伦药业在审评审批中的一致性评价补充申请
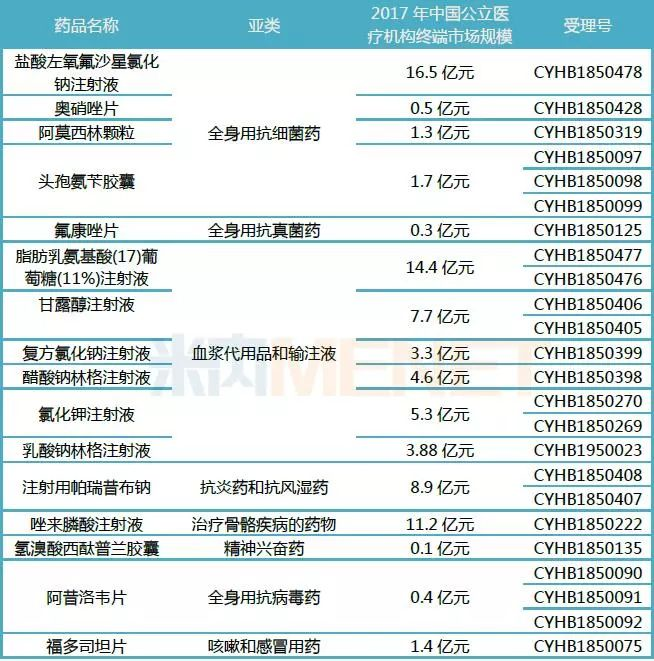
(来源:米内网MED中国药品审评数据库2.0)
截至2019年1月18日,通过一致性评价的产品主要为口服剂型,注射剂仅有8个。科伦药业在审评审批的16个产品中有9个为注射剂。
据米内网数据显示,2017年在中国公立医疗机构终端,盐酸左氧氟沙星氯化钠注射液、脂肪乳氨基酸(17)葡萄糖(11%)注射液、唑来膦酸注射液的销售额均破十亿。
盐酸左氧氟沙星氯化钠注射液的领军企业为扬子江药业集团,市场份额占51.19%,TOP2企业四川科伦药业占20.65%。目前仅有四川科伦药业的一致性评价补充申请在审评审批中。
脂肪乳氨基酸(17)葡萄糖(11%)注射液的领军企业为费森尤斯卡比华瑞制药,目前仅有四川科伦药业的一致性评价补充申请在审评审批中。
唑来膦酸注射液的领军企业为诺华,市场份额占47.59%,目前仅有四川科伦药业的一致性评价补充申请在审评审批中。
此外,目前仅有科伦药业提交一致性评价补充申请的产品还有奥硝唑片、甘露醇注射液、复方氯化钠注射液、氯化钾注射液。氢溴酸西酞普兰胶囊为科伦药业的独家产品,目前该产品的一致性评价补充申请正在审评审批中。
值得注意的是,科伦药业的注射用帕瑞昔布钠一致性评价补充申请曾在2018年7月30日被承办,2018年11月9日发件,但暂无结论。此次两个受理号的承办日期均为2018年12月13日,目前正在审评审批中。齐鲁制药的注射用帕瑞昔布钠一致性评价补充申请在2018年8月14日被承办,目前正在审评审批中,最终哪家企业的产品能突围成功,我们继续关注。
3个1类新药已获批临床,两个为注射剂
表3:科伦药业2018年获批临床的1类新药
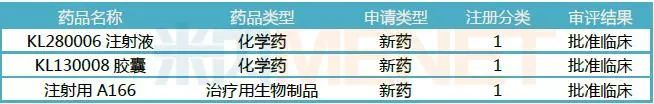
(来源:MED中国药品审评数据库2.0)
KL280006注射液为科伦药业研发的具有自主知识产权的选择性外周κ阿片受体激动剂,实现有效镇痛的同时能避免中枢镇痛类药物的不良反应,拟用于急性疼痛(如术后疼痛)的治疗。非临床研究数据证实KL280006注射液作用机制明确,对外周κ受体具有高亲和性和高选择性,不易透过血脑屏障,镇痛效果确切,兼具良好的安全性和耐受性,无心脏、呼吸及中枢神经系统等不良反应。目前,全球尚无外周选择性κ受体激动剂类药物获批上市。截至2018年7月,公司在KL280006注射液研发项目上已投入研发费用约800万元。
KL130008胶囊为小分子JAK抑制剂,通过JAK-STAT信号通路实现免疫调节,拟用于类风湿关节炎的治疗。非临床研究数据表明,KL130008作用机制明确,高效选择性抑制JAK激酶活性,实现显著缓解类风湿关节炎病情的同时,兼具良好的安全性和耐受性。全球用于类风湿关节炎治疗的JAK抑制剂目前已上市Tofacitinib(枸橼酸托法替布片)和 Baricitinib(巴瑞克替尼)。辉瑞的枸橼酸托法替布片于2017年在国内获批上市。截至2018年6月,公司在该研发项目上已投入研发费用约760万元。
注射用A166是全球首个通过赖氨酸定点定量偶联、具有创新连接子和高活性毒素小分子的第三代抗HER2 ADC,拟用于HER2阳性乳腺癌、胃癌等恶性肿瘤的治疗。非临床研究数据表明,注射用A166可在温和条件下实现定点定量偶联,无需抗体工程化改造、修饰或还原,免疫原性风险低;在不同HER2表达水平及赫赛汀耐药动物肿瘤模型中的抗肿瘤活性显著优于同类已上市药物,且具有良好的血液稳定性和肿瘤靶向性,实现高活性毒素载荷的同时,兼具良好的安全性和耐受性。全球以HER2为靶点的ADC药物仅有罗氏的KADCYLA®(T-DM1),于2013年经FDA批准上市,暂未在国内上市。截至2018年5月,公司在注射用A166研发项目上已投入研发费用约3200万元。
结语
作为大输液的龙头企业,科伦药业在“限输限抗”的政策压力下调整战略,大力推动非输液业务的发展,目前来看效果可喜。在2018年一致性评价+带量采购带来的行业洗牌中,科伦药业也跟上了新政的节奏,6个产品顺利通过一致性评价,草酸艾司西酞普兰片中标4+7带量采购,目前仍有16个产品的一致性评价在审。从目前的情况来看,注射剂的审评工作愈趋严格,科伦药业2019年过评产品又会有哪些?我们拭目以待。
资料来源:米内网数据库、上市公司公告
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..